Síra: Vlastnosti, Reakcie a Význam v Prírode i Priemysle
Síra (chemická značka S, latinsky sulphur) je nekovový chemický prvok žltej farby, pomerne hojne zastúpený v prírode. Patrí medzi chalkogény, nachádza sa v skupine VI A (16. skupina) Periodickej tabuľky prvkov a má protónové číslo 16.
Fyzikálne vlastnosti síry
Síra je krehký nekov žltej farby, známy od staroveku. Pri normálnej teplote je síra tuhá žltá látka s veľmi slabým, charakteristickým zápachom. Je nerozpustná vo vode, málo rozpustná v nepolárnych rozpúšťadlách ako benzén či toluén, ale dobre rozpustná v sírouhlíku.
Síra taje pri teplote 114 °C za vzniku žltej priehľadnej kvapaliny, nazývanej kapalná síra. Pri zahrievaní nad kahanom dochádza k roztaveniu práškovej síry vo žltú kvapalinu, ktorá začne postupne tmavnúť (hnedé sfarbenie), pričom vzrastá viskozita. Pri určitej teplote (okolo 200 °C) je viskozita tak vysoká, že možno skúmavku otočiť dnom nahor. Pri ďalšom zahrievaní viskozita klesá. Pri teplote 444 °C síra vrie a uvoľňuje oranžové pary.

Charakteristické javy vyskytujúce sa pri zahrievaní roztavenej síry možno vysvetliť prítomnosťou troch modifikácií Sλ, Sμ a Sπ v kvapalnej síre. Ku zmene sfarbenia kvapalnej síry zo žltej na hnedú dochádza zrejme preto, že Sλ je žltá a Sμ temne hnedočervená. Zmena viskozity spojená so zahrievaním sa dá vysvetliť aj tým, že Sμ je viskóznejšia a Sπ vznikajúca pri vyšších teplotách je menej viskózna. Viskozita Sμ so vzrastajúcou teplotou klesá. Vzrast koncentrácie Sμ zvyšuje viskozitu tak dlho, až konečne s ďalej zvyšujúcou sa teplotou viskozita Sμ klesá rýchlejšie, než rastie koncentrácia Sμ.
Alotropické modifikácie síry
Síra sa vyskytuje v niekoľkých alotropických modifikáciách. Základnou modifikáciou je kosoštvorcová (rhombická) - Sα, ktorá je najbežnejšia a najstabilnejšia. Na ňu postupne prechádzajú všetky ostatné modifikácie. Jedná sa o žltú krystalickú látku, ktorá je monocyklická osmiatomová - tvorená 8 atómami síry spojenými do kruhu. Kosočtverečná (α) je stálá modifikácia, žlutá látka nerozpustná ve vodě, dobře rozpustná v sirouhlíku, v ethanolu nebo etheru.

Pri teplote cca 95 °C prechádza kosoštvorcová modifikácia na jednoklonnú (monoklinickú) - Sβ. Táto modifikácia sa pripraví kryštalizáciou kvapalnej síry pri teplote 100 °C a rýchlym ochladením na teplotu cca 20 °C. Jednoklonná modifikácia síry Sβ je tvorená ihličkovitými kryštálmi. Po čase táto modifikácia prechádza v kosoštvorcovú.
Jednoklonná (monoklinická) modifikácia Sγ sa pripravuje pomalým ochladzovaním taveniny síry z teploty 150 °C. Táto modifikácia tiež pomaly prechádza v Sα.
Kosoštvorcová aj jednoklonná síra sú tvorené cyklickými molekulami S8 (8 atómov síry spojených do kruhu). Vzájomne sa líšia iba usporiadaním týchto molekúl v kryštalickej štruktúre.
Síra taje pri teplote 114 °C, osmičlenné kruhy sa porušujú a spájajú sa do dlhých reťazcov Sn alebo S∞ - vzniká kvapalná síra. Prudkým ochladením (napr. vyliatím slabým prúdom do studenej vody) horúcej kvapalnej síry z teploty okolo 400 °C možno pripraviť plastickú síru (označovanú ako Sλ - amorfná modifikácia rozpustná v sírouhlíku, Sμ - amorfná modifikácia nerozpustná v sírouhlíku, plastická síra môže ešte obsahovať za určitých podmienok modifikáciu Sπ). Jedná sa o žltohnedú, tvárnu a pružnú hmotu. Molekuly plastickej síry vytvárajú dlhé polymérne reťazce, ktoré sú tiež príčinou jej plastickosti. Plastická síra časom prechádza v kosoštvorcovú modifikáciu.
Rýchlym ochladením pár síry vzniká sírny kvet, ktorý má podobu žltého prášku. Síra je tiež súčasťou pušného prachu.
Sugar + Sulfuric Acid ⚠ Experiment
Chemické vlastnosti a reakcie síry
Síra je pomerne reaktívny prvok. Horí modrastým plameňom za vzniku oxidu siričitého SO2. Priamo sa zlučuje so všetkými prvkami okrem vzácnych plynov, dusíka, telúru, jódu, irídia, platiny a zlata.
- Reakcie s kyslíkom: S čistým kyslíkom síra za normálnej teploty nereaguje. Horí modrastým plameňom na oxid siričitý, ktorý má ostrý, štipľavý zápach, bieliace a dezinfekčné účinky.
- Reakcie s vodíkom: Pri teplote 120 °C veľmi pomaly reaguje s vodíkom za vzniku sírovodíka (sulfánu) H2S. Sulfán je veľmi jedovatý (smrteľne toxická koncentrácia vo vzduchu 0,15 %) plyn silne zapáchajúci po zkažených vajciach.
- Reakcie s halogénmi: V atmosfére plynného fluóru sa síra vznítí za vzniku SF6. Reakcia s ďalšími halogénmi prebieha pri normálnej teplote kľudne.
- Reakcie s kovmi: S kovmi reaguje za vzniku farebných sulfidov. Napríklad, strieborný sulfid je čierny, olovnatý čierny, bizmutitý hnedý, antimonitý oranžový, kademnatý žltý, zinočnatý biely.
Vo zlúčeninách síra najčastejšie zaujíma oxidačné číslo -II (v sulfidoch), IV a VI. Menej obvyklá sú oxidačné čísla -I (disulfidy a okrajové atómy síry u polysulfidov), 0 (vnútorné atómy síry v polysulfidoch) a I. Na rozdiel od kyslíka môže síra zasahovať do d-orbitalu. Atómy síry môžu existovať v excitovanom stave prvého stupňa S* (štvorväzný s oxidačným číslom +IV) a druhého stupňa S** (šesťväzný s oxidačným číslom +VI). Síra najčastejšie tvorí kovalentné väzby (jednoduché, dvojné), v organických látkach je významná väzba koordinačno-kovalentná, v ktorej atómy síry majú rolu donora (darcu).
Výskyt síry v prírode a jej ťažba
Síra tvorí približne 0,03-0,09 % zemskej kôry, v morskej vode sa jej koncentrácia pohybuje okolo 900 mg/l. Ako čistý prvok sa vyskytuje predovšetkým v oblastiach s bohatou vulkanickou činnosťou alebo v okolí horúcich minerálnych prameňov. V prírode sa voľná síra vyskytuje v sopečných kráteroch na Sicílii a v ložiskách v hĺbke zeme v Louisiane, Poľsku, Grécku, Japonsku, Kaukaze a na Urale.
Častejšie sa síra vyskytuje v sulfidoch, ako sú pyrit (disulfid železnatý), galenit (sulfid olovnatý), sfalerit (sulfid zinočnatý), antimonit, chalkopyrit (zmesný sulfid medi a železa) a cinabarit (sulfid rtuťnatý - rumelka). Taktiež sa nachádza v síranoch ako sadrovec, baryt a alumit.
Hlavné oblasti ťažby síry sú Poľsko, Povolžie, Kazachstán a USA. Na Sicílii sa rýdza síra získava zo sopečných kameňov topením a odlievaním do kolíkov. V Louisiane sa po roztopení horúcou parou vytláča z podzemných ložísk tlakom vzduchu. Síra sa získava aj zo sadry, barytu a svietiplynu. Naprostá väčšina zo svetovej ročnej produkcie (64 miliónov ton síry v roku 2005) vzniká ako vedľajší produkt pri odsírovaní ropy a zemného plynu. Využíva sa pri tom predovšetkým tzv. Clausov proces a jeho modifikácie.
Význam síry pre živé organizmy
Síra je podstatnou zložkou organických materiálov a vyskytuje sa v rôznych bielkovinách ako aminokyselina cysteín či metionín, prítomných prakticky vo všetkých živých organizmoch. Je súčasťou každej bunky tela, pretože sa nachádza v aminokyselinách, a preto aj v bielkovinách a enzýmoch. Tvorí súčasť niektorých vitamínov (biotín, kyselina lipoová, tiamín), koenzýmu A, heparínu, glutatiónu, lipidov v mozgu atď. Reťazce inzulínu sú navzájom viazané dvoma disulfidovými väzbami.
Dále síra tvorí v proteínoch Fe-S štruktúry, je súčasťou koenzýmu A a rôznych vitamínov. Vyskytuje sa v glutathióne, ktorý dokáže inaktivovať rôzne toxíny. Glutathión je zložkou fytochelatínov, ktoré dokážu vyvazovať z pôdy ťažké kovy. Zaujímavosťou je, že glutathión nevzniká bežným procesom proteosyntézy na ribozómoch, ale činnosťou špeciálnych enzýmov, aktivovaných ťažkými kovmi.
Rastliny prijímajú síru z pôdy vo vodnom roztoku ako síranový anión SO4(2-) symportom s tromi protónmi H+. Tieto protóny musia byť potom zasa vyčerpané ATPázovými pumpami von z bunky za investície ATP, aby sa udržala ich optimálna koncentrácia v bunke. Príjem síry je pre rastlinu energeticky náročný.
Do organizmu sa síra dostáva najčastejšie v potrave bohatej na bielkoviny (syry, strukoviny, vajcia). V ľudkom organizme je malé množstvo síry prítomné aj vo forme síranov (sodných alebo draselných) v krvi a tkanivách. Najmä v moči je prítomná vo forme síranov. Zlúčeniny síry nachádzajúce sa v cesnaku siatom, napríklad aliín, alicín, alycysteín a iné sa dostávajú do krvi niekoľko minút po použití.
Nedostatok síry v našich podmienkach nehrozí. Hoci síra a jej zlúčeniny majú charakteristický nepríjemný zápach, pre človeka nepredstavuje až také nebezpečenstvo, ako iné látky, ktoré majú tiež výrazný zápach.
Použitie síry a jej zlúčenín
Síra bola známa už v dávnoveku a napríklad v starovekej Číne slúžila ako jedna zo zložiek strelného prachu. Síra má široké uplatnenie v modernom priemysle. Využíva sa pri vulkanizácii kaučuku, ktorý sa po zmiešaní so sírou a zahriatí stáva pružným a dobre udržuje tvar. Množstvo síry pridanej do zmesi potom určuje tvrdosť získaného produktu.
Síra je významnou zložkou rôznych fungicídov, teda prostriedkov pôsobiacich proti rastu húb a plesní. Dříve sa používala pre výrobu zápaliek. Keďže je horľavá, používa sa pri výrobe zápaliek, pušného prachu a náplní pre ohňostroje.
Jej zlúčenina, kyselina sírová, je jednou z chemikálií s najširším použitím v chemickom priemysle. Kyselina sírová je základnou surovinou pri výrobe kyseliny chlorovodíkovej a dusičnej, hnojív, pri rafinácii ropy.
V chemickom priemysle sa elementárna síra používa predovšetkým pre vulkanizáciu kaučuku, pri výrobe papiera, pri dezinfekcii vo viniciach a potravinárskom priemysle, pri výrobe sodného skla, pri úprave rúd a výrobe hnojív, vo fungicídoch, ale je aj súčasťou zápaliek. Vo farmácii sa síra využíva na výrobu rôznych mastí a kúpeľných prípravkov. Vo fotografii sa uplatňuje siričitan a tiosíran sodný na prípravu vývojiek a ustalovačov.

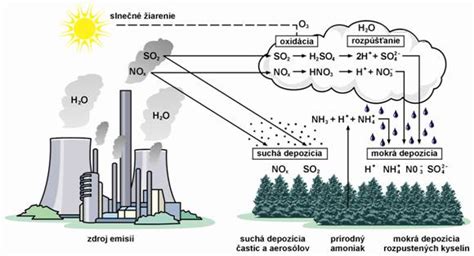
Vplyv síry na životné prostredie a kyslé dažde
V atmosfére je síra prítomná vo forme svojich oxidov, predovšetkým siričitého, ale aj sírového. Pred rokom 1989 bol oxid siričitý hlavným problémom kvality ovzdušia, predovšetkým v dôsledku masívneho spaľovania uhlia s vysokým obsahom síry. Reakciou s vodnou parou obsiahnutou v atmosfére vznikajú kyseliny siričitá a sírová, ktoré sa podieľajú na vzniku kyslých dažďov, ktoré sa podieľali na zničení smrekových lesov napríklad Jizerských a Krušných hôr.
Medzi rokmi 1990 až 2006 došlo v Českej republike k poklesu emisií SO2 takmer o 90 % v dôsledku inštalácii účinných odsírovacích zariadení, väčšinou za použitia alkalických sorbentov (mletý vápenec alebo magnezit).